당뇨가 있다면 공복혈당보다 ‘이것’을 먼저 확인하세요
혈당 변동성과 치매 위험 — 당화혈색소가 정상이어도 안심할 수 없는 이유
진료실에서 이런 상황을 마주하는 경우가 있습니다. 당화혈색소(HbA1c)가 6.8%로 비교적 잘 관리되고 있다는 이야기를 들어온 67세 여성 환자가 최근 들어 자꾸 깜빡하고, 대화 중에 단어가 떠오르지 않는다고 호소하며 내원했습니다. 당뇨약도 규칙적으로 복용하고, 정기검진에서도 혈당 관리가 양호하다는 평가를 받아왔습니다. 그런데 왜 인지 기능에 문제가 생기는 것일까요.
이 질문의 답은 ‘혈당의 평균값’이 아니라 ‘혈당이 얼마나 들쑥날쑥한가’에 있을 가능성이 있습니다. 당화혈색소는 지난 2~3개월간의 혈당 평균을 반영하는 지표입니다. 그러나 매일 반복되는 식후 혈당 스파이크와 야간 저혈당은 이 평균값에 묻혀 보이지 않습니다. 최근 연구들은 이 ‘혈당의 오르내림 폭’, 즉 혈당 변동성이 뇌 건강에 미치는 영향이 평균 혈당만큼, 혹은 그 이상으로 중요할 수 있다는 점을 보고하고 있습니다.
이 칼럼은 당뇨와 치매의 연관성, 혈당 변동성이 뇌에 어떤 손상을 일으키는지의 기전, 그리고 일상에서 혈당 변동성을 줄이기 위해 실천할 수 있는 구체적인 방법을 담았습니다. 당뇨를 진단받으셨거나, 가족 중 당뇨와 인지 기능 저하를 함께 걱정하시는 분들을 위해 가능한 한 상세하게 정리했습니다.

1. 당뇨와 치매 — 위험 수치가 말하는 것
당뇨는 치매의 위험 인자입니다 — 수십 개 연구가 일치하는 결론
당뇨병과 치매의 연관성은 오랜 기간 다수의 역학 연구를 통해 축적된 결론입니다. 144개의 전향적 코호트 연구, 9백만 명 이상의 데이터를 포함한 대규모 메타분석에서 당뇨병 환자의 전체 치매 위험은 비당뇨인 대비 약 1.73배 높았으며, 혈관성 치매의 위험은 2.27배까지 상승했습니다.¹ 이 수치는 단순히 통계적 연관성이 아닙니다. 연령, 고혈압, 고지혈증, 비만 등 혼란 변수를 보정한 후에도 유의미하게 유지된다는 점에서 당뇨 자체가 뇌에 독립적인 영향을 미친다는 것을 시사합니다.
혈관성 치매보다 알츠하이머병은 당뇨와의 연관성이 상대적으로 덜 강한 것으로 알려져 있었으나, 최근 연구들은 이 관계도 재평가되고 있습니다. 뇌의 인슐린 저항성이 아밀로이드 베타 축적과 타우 단백질 인산화 — 알츠하이머의 핵심 병리 — 에 직접 관여한다는 기전이 밝혀지고 있기 때문입니다.

당뇨 발병 나이가 빠를수록 치매 위험이 더 높아집니다
한국 국민건강보험 데이터를 활용한 대규모 연구(61만 2,201명)에서 특히 주목할 만한 결과가 나왔습니다. 2형 당뇨를 50세 이전에 진단받은 경우 전체 치매 위험이 대조군 대비 3.29배, 알츠하이머병은 4.08배, 혈관성 치매는 5.82배까지 상승했습니다.² 60대 이후 진단 시에는 이 위험비가 점차 감소합니다.
이 결과는 중요한 메시지를 담고 있습니다. 40~50대에 당뇨를 진단받은 분들은 치매 예방이라는 관점에서도 혈당 관리를 조기에, 그리고 장기적으로 유지하는 것이 특히 중요합니다. 노년기 당뇨보다 중년기 당뇨가 뇌에 더 오래 영향을 미치기 때문입니다.
당뇨와 치매 위험도 — 주요 연구 데이터 요약
| 연구 / 데이터 | 치매 유형 | 위험비 (RR/HR) | 출처 |
|---|---|---|---|
| 28개 코호트 메타분석(20만 명 이상) | 전체 치매 | RR 1.73 (1.65–1.82) | Xue et al. 2019, Ageing Res Rev |
| 동일 메타분석 | 혈관성 치매 | RR 2.27 (1.94–2.66) | Xue et al. 2019 |
| 한국 코호트(61만 2천 명) | 전체 치매(50세 이전 진단 시) | HR 3.29 (3.11–3.49) | PMC 2024, NHIS 데이터 |
| 동일 한국 코호트 | 알츠하이머(50세 이전 진단 시) | HR 4.08 (3.18–5.24) | PMC 2024, NHIS 데이터 |
| 스웨덴 코호트(4만 3,440명 1형 당뇨) | 전체 치매 | HR 2.02 (1.83–2.23) | Jancev et al. 2025, Diabetes Care |
| HbA1c 변동성 코호트(17만 1,964명) | 전체 치매(HbA1c 정상 범위에서도) | HR 1.15 per SD 상승→ 최고 분위 15% 위험 증가 | Rawlings et al. 2024, Alzheimers Dement |
| 당뇨병이 있는데 이런 증상이 있다면 인지 기능 평가를 권유합니다 • 대화 중 단어가 갑자기 생각나지 않는 경우가 잦아진 경우 • 최근 있었던 일을 반복적으로 질문하거나 기억하지 못하는 경우 • 익숙한 길이나 장소에서 방향 감각이 흐려지는 경우 • 복잡한 계산이나 계획 수립이 이전보다 어려워진 경우 • 성격이나 감정 반응이 달라졌다는 이야기를 주변에서 듣는 경우이 증상들이 혈당 조절 상태와 무관하게 나타난다면 더욱 주의가 필요합니다. |
[이미지 삽입 위치: 2 — 뇌 MRI 또는 신경세포 관련 의학 일러스트]
2. 혈당 변동성 — 평균 혈당보다 더 위험할 수 있습니다
당화혈색소가 정상이어도 안심할 수 없는 이유
당화혈색소(HbA1c)는 현재 당뇨 관리의 핵심 지표입니다. 이 수치가 목표 범위(일반적으로 7% 이하) 안에 있으면 혈당이 잘 관리되고 있다고 평가합니다. 그러나 HbA1c는 구조적인 한계가 있습니다. 적혈구의 수명인 약 2~3개월 동안의 혈당 평균을 반영하기 때문에, 그 사이에 반복된 혈당 스파이크와 저혈당은 평균값에 상쇄되어 보이지 않습니다.
예를 들어, 매 식후 혈당이 220mg/dL까지 치솟지만 두 시간 후 빠르게 떨어지는 패턴과, 혈당이 140~180mg/dL 사이에서 안정적으로 유지되는 패턴이 동일한 HbA1c 수치를 만들어낼 수 있습니다. 두 패턴의 평균값은 같지만, 뇌에 가해지는 손상은 전혀 다릅니다.
HbA1c 변동성이 치매 위험을 독립적으로 높인다 — 17만 명 연구
영국의 대규모 전자건강기록 코호트 연구(17만 1,964명)에서 방문마다 측정한 HbA1c의 표준편차, 즉 장기적 변동성이 클수록 치매 발생 위험이 유의미하게 증가한다는 결과가 발표되었습니다.³ 핵심적인 발견은 HbA1c 평균값이 6~8% 사이의 정상 범위에 있는 사람들에서도 변동성이 클 경우 치매 위험이 의미 있게 높았다는 점입니다.
또한 하루하루의 공복혈당 변동성을 5년간 추적한 한국 코호트 연구(76만 9,554명)에서 공복혈당 변동성이 가장 높은 군은 가장 낮은 군 대비 전체 치매 위험이 18%, 알츠하이머 위험이 19% 높았습니다.⁴ 이 수치는 수십만 명 단위 추적 데이터에서 나온 것으로, 통계적 신뢰도가 높습니다.
당화혈색소(HbA1c)와 혈당 변동성 — 무엇이 다른가
| 항목 | 당화혈색소 (HbA1c) | 혈당 변동성 (GV) |
|---|---|---|
| 측정 대상 | 지난 2~3개월간 평균 혈당 | 혈당이 얼마나 들쑥날쑥한지의 정도 |
| 측정 방법 | 3개월마다 혈액검사 한 번 | 연속혈당측정기(CGM) 또는 반복 자가혈당측정 |
| 놓치는 정보 | 식후 혈당 스파이크, 야간 저혈당을 반영 못함 | 평균값은 정상이지만 스파이크가 반복될 때 포착 가능 |
| 치매 예측력 | HbA1c 자체는 치매와 연관되나, 정상 범위에서는 예측 한계 있음 | HbA1c 정상 범위에서도 변동성이 크면 치매 위험 유의미하게 증가 |
| 임상 활용 | 현재 표준 혈당 관리 지표 | CGM 보급과 함께 중요성 점증 중 |
혈당 변동성이 뇌를 손상시키는 세 가지 경로

경로 1 — 산화 스트레스와 뇌혈관 손상
혈당이 급격히 상승하면 미토콘드리아 전자 전달계에 과부하가 걸리면서 활성산소(ROS)가 과다 생성됩니다. 이 산화 스트레스는 혈관 내피세포를 손상시키고, 뇌소혈관의 경직과 협착을 유발합니다. 혈당이 안정적으로 유지될 때보다 혈당이 같은 평균값이라도 급격히 오르내릴 때 산화 스트레스가 더 크게 발생한다는 점이 핵심입니다.⁵
뇌 MRI에서 확인되는 백질 병변(white matter hyperintensity)은 이 과정의 결과물입니다. 혈당 변동성이 클수록 백질 병변 부담이 증가하며, 이는 집행 기능 저하, 처리 속도 감소, 기억력 감퇴와 연관됩니다. 백질 병변은 치매의 전구 병리로 간주되며, 한번 발생한 병변은 가역적 회복이 어렵습니다.
경로 2 — 아밀로이드 베타 축적과 타우 인산화
혈당 변동성이 큰 상태에서는 뇌의 인슐린 신호 전달이 불안정해집니다. 인슐린 분해 효소(IDE, Insulin Degrading Enzyme)는 아밀로이드 베타의 분해도 담당하는데, 인슐린 신호 이상 상태에서는 이 효소의 기능이 저하됩니다. 그 결과 아밀로이드 베타가 뇌에 축적되기 쉬운 환경이 만들어집니다.⁶
동시에 혈당 변동성은 타우 단백질의 과도한 인산화를 촉진합니다. 정상 타우는 신경세포의 내부 골격을 유지하는 단백질이지만, 과인산화된 타우는 신경섬유매듭(neurofibrillary tangle)을 형성하여 신경세포를 죽입니다. 이 두 병리 — 아밀로이드 반과 신경섬유매듭 — 는 알츠하이머병의 핵심 병리 소견입니다. 혈당 변동성이 이 두 가지 모두에 기여할 수 있다는 점에서, 혈당 관리는 단순한 합병증 예방을 넘어 알츠하이머 예방의 영역에 걸쳐 있습니다.
경로 3 — 저혈당의 직접적 신경 손상
혈당 변동성의 또 다른 측면은 저혈당입니다. 뇌는 전체 체중의 2%에 불과하지만 안정 시 전체 포도당 소비의 약 20%를 사용하는 에너지 집약 기관입니다. 혈당이 70mg/dL 이하로 떨어지면 뇌는 에너지 공급 부족에 빠집니다. 이 상태가 반복되거나 심각해지면 신경세포의 직접 손상이 발생합니다.
한국 국민당뇨병 프로그램 코호트 분석에서 노인 2형 당뇨 환자 중 심한 저혈당을 경험한 군에서 치매 발생 위험이 유의미하게 증가했습니다.⁷ 특히 야간 저혈당은 본인이 인지하지 못한 채 지나가는 경우가 많아 더 위험합니다. 당뇨 치료 중 저혈당이 잦다면 치매 위험 감소를 위해서도 혈당 조절 방식을 재검토할 필요가 있습니다.
| 혈당 변동성이 뇌에 미치는 손상 — 3가지 경로 요약 • 혈당 스파이크 → 활성산소 과다 생성 → 뇌소혈관 내피 손상 → 백질 병변 → 인지 기능 저하 • 혈당 불안정 → 뇌 인슐린 신호 장애 → 아밀로이드 베타 축적 + 타우 과인산화 → 알츠하이머 병리 • 반복적 저혈당 → 뇌세포 에너지 고갈 → 신경세포 직접 손상 → 인지 기능 감퇴 세 경로 모두 HbA1c가 정상 범위에 있더라도 혈당 변동성이 크다면 진행될 수 있습니다. |
3. 뇌 인슐린 저항성 — 알츠하이머를 ‘제3형 당뇨’라 부르는 이유
뇌에도 인슐린 수용체가 있습니다
인슐린은 혈당을 낮추는 호르몬으로만 알려져 있지만, 사실 뇌에서도 중요한 역할을 합니다. 뇌의 인슐린 수용체는 기억과 학습을 담당하는 해마, 인지 기능의 중추인 대뇌피질, 감정 조절의 시상하부에 특히 풍부하게 분포합니다.⁶ 인슐린은 뇌에서 신경세포 생존을 촉진하고, 시냅스 가소성을 유지하며, 아밀로이드 베타 분해에도 관여합니다. 혈당 조절과 별개로 뇌에서 인슐린 신호 자체가 제대로 작동해야 인지 기능이 유지된다는 의미입니다.
뇌의 인슐린 저항성 — 뇌세포가 포도당을 제대로 쓰지 못하는 상태
만성적인 고혈당과 혈당 변동성이 지속되면 뇌세포에서도 인슐린 저항성이 발생할 수 있습니다. 뇌세포가 인슐린 신호에 둔감해지면서 포도당 운반체(GLUT3)의 발현이 감소합니다. 그 결과 혈중에 포도당이 충분히 있어도 뇌세포는 이를 제대로 흡수하여 에너지로 사용하지 못하는 ‘뇌의 에너지 기근’ 상태가 됩니다.
PET 영상 연구들은 알츠하이머 환자에서 뇌 포도당 대사가 현저히 감소한다는 사실을 일관되게 보여주고 있습니다. 더 놀라운 것은 이 뇌 포도당 대사 감소가 알츠하이머 증상이 나타나기 10년 이상 전부터 시작된다는 점입니다.⁶ 즉, 인지 기능이 겉으로는 멀쩡해 보이는 시기에 이미 뇌에서는 에너지 대사 이상이 진행되고 있습니다.
왜 ‘제3형 당뇨’라는 개념이 등장했는가
뇌의 인슐린 저항성과 알츠하이머의 연관성이 점차 확인되면서, 일부 연구자들은 알츠하이머를 ‘뇌에서 발생한 당뇨’, 즉 ‘제3형 당뇨’로 명명하기 시작했습니다. 이 개념은 알츠하이머가 단순히 노화의 산물이 아니라, 뇌의 인슐린 신호 장애와 포도당 대사 이상이 축적된 결과일 수 있다는 관점입니다.⁶
이 개념은 아직 학술적으로 완전히 확립된 것은 아닙니다. 그러나 이 관점이 중요한 이유는 당뇨 환자에서 혈당 변동성을 줄이는 것이 단지 신장·눈·발 등의 합병증을 예방하는 것을 넘어, 뇌 자체를 보호하는 적극적인 개입이 될 수 있다는 논거를 제공하기 때문입니다.
혈당 조절이 개선되면 뇌 포도당 대사도 회복될 수 있습니다
긍정적인 연구 결과도 있습니다. 혈당 조절이 개선된 2형 당뇨 환자에서 뇌의 포도당 운반체(GLUT) 기능과 뇌 포도당 대사가 부분적으로 회복되는 것이 관찰되었습니다.⁵ 이는 뇌의 에너지 대사 저하가 어느 정도까지는 가역적일 수 있음을 시사합니다. 당뇨 진단 이후에도 혈당 변동성을 적극적으로 줄이는 노력이 늦지 않다는 의미이기도 합니다.
4. 혈당 변동성을 줄이는 실천 방법 — 기전과 함께 이해하면 지속됩니다
혈당 변동성 관리는 단순히 단 것을 줄이는 것이 아닙니다. 혈당이 얼마나 빠르게 올라가느냐, 식후 얼마나 오래 높은 상태가 유지되느냐, 그리고 저혈당이 반복되지는 않는지 — 이 세 가지를 동시에 관리해야 합니다. 아래에 설명하는 방법들은 각각 기전이 있습니다. 왜 효과가 있는지를 이해하면 실천하기가 훨씬 수월해집니다.

식사 순서 변경 — 같은 음식, 다른 혈당 반응
식사를 어떤 순서로 먹느냐에 따라 같은 음식을 먹어도 식후 혈당의 피크 높이가 달라집니다. 채소를 먼저 먹으면 식이섬유가 위와 소장에서 젤 형태의 막을 형성합니다. 이 막은 이후 섭취하는 탄수화물의 소화·흡수 속도를 늦춥니다. 단백질을 먼저 먹으면 인슐린보다 먼저 GLP-1(글루카곤 유사 펩타이드-1)이 분비되어 위 배출 속도가 느려지고, 인슐린 분비 타이밍도 혈당 상승에 더 잘 맞춰집니다.
권장 순서는 채소 → 단백질(두부·생선·달걀·콩류) → 탄수화물(밥·빵·면)입니다. 밥을 먼저 먹던 습관을 바꾸는 것만으로 식후 혈당 스파이크가 20~40% 감소하는 경향이 관찰됩니다. 이 방법의 장점은 섭취하는 음식 자체를 바꾸지 않고 순서만 조정한다는 것입니다.
식후 보행 — 근육이 혈당을 흡수합니다
식후 15~20분 이내에 10~15분 정도 걷는 습관은 혈당 변동성 감소에 실질적인 효과가 있습니다. 근육이 수축할 때는 인슐린 없이도 GLUT4라는 포도당 운반체가 근육세포 표면으로 이동하여 혈중 포도당을 직접 흡수합니다. 즉, 인슐린이 부족하거나 저항성이 있는 상태에서도 근육 수축 자체가 혈당을 낮추는 독립적인 경로가 됩니다.
식후 바로 보행하는 것이 운동 효과에서 중요한 이유는 타이밍입니다. 식후 혈당은 30~60분 사이에 최고치에 달합니다. 이 상승 구간을 보행으로 차단하면 피크 자체가 낮아지고, 이후 혈당이 급격히 떨어지는 것도 완화됩니다. 산책 수준의 걸음으로도 효과가 있으며, 격렬한 운동일 필요는 없습니다.
저혈당 예방 — 과도한 치료의 역설
저혈당을 예방하는 것은 혈당을 낮게 유지하는 것과 다릅니다. 당뇨 약물 치료 중 혈당이 지나치게 공격적으로 낮춰지거나, 식사를 거르거나, 운동량이 갑자기 늘어난 경우 저혈당이 발생합니다. 특히 고령의 당뇨 환자에서 야간 저혈당은 증상 없이 지나가는 경우가 많습니다.
저혈당이 뇌에 미치는 손상은 고혈당과 다른 기전입니다. 고혈당이 산화 스트레스와 혈관 손상을 통해 점진적으로 작용한다면, 저혈당은 뇌세포에 에너지가 급격히 공급되지 않아 직접적·즉각적인 신경 손상을 일으킵니다. 심한 저혈당을 한 번 경험하는 것만으로도 인지 기능에 영향을 줄 수 있다는 보고가 있습니다. 현재 당뇨 치료 중 저혈당 삽화가 잦다면 목표 혈당 범위를 재조정하는 것을 담당 의사와 상담하는 것이 권장됩니다.
수면 — 혈당 변동성 관리의 숨은 변수
수면과 혈당 조절의 관계는 생각보다 긴밀합니다. 수면이 부족하면 코르티솔과 성장호르몬 분비 패턴이 교란되어 인슐린 저항성이 증가하고, 이는 공복혈당 상승으로 이어집니다. 또한 수면 중에는 뇌의 노폐물 청소 시스템인 글림프 시스템(glymphatic system)이 활성화되는데, 이 시스템은 뇌에 축적된 아밀로이드 베타를 제거하는 역할을 합니다. 수면 부족은 이 청소 과정을 방해하여 아밀로이드 베타가 뇌에 더 많이 남게 됩니다.
하루 7~8시간의 규칙적인 수면을 유지하는 것이 혈당 안정화와 뇌 건강 모두에 도움이 됩니다. 특히 수면무호흡증이 있는 경우 야간 혈당 변동성이 커지고 산소 포화도 저하가 뇌혈관에 추가적인 손상을 줄 수 있으므로, 코골이나 수면 중 호흡 장애가 의심되면 수면 검사를 받아보는 것이 권장됩니다.
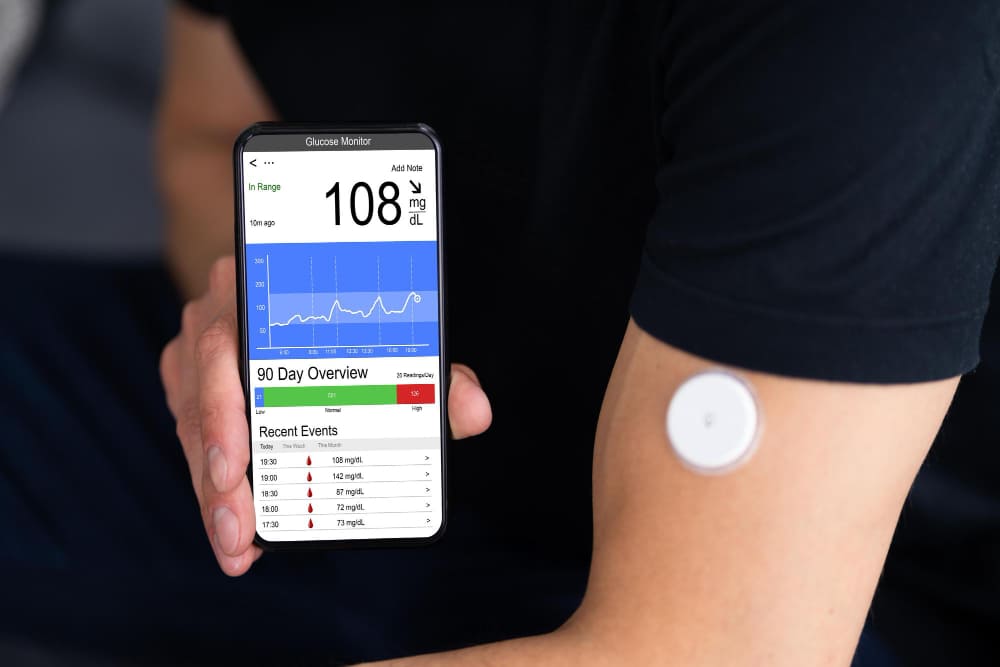
연속혈당측정기(CGM) — HbA1c의 사각지대를 채우는 도구
연속혈당측정기(Continuous Glucose Monitor, CGM)는 피부 아래 센서를 통해 하루 24시간 실시간으로 혈당을 측정하는 기기입니다. 3개월마다 한 번의 혈액검사로 확인하는 HbA1c와 달리, CGM은 식사에 따른 혈당 상승 패턴, 야간 저혈당, 새벽 혈당 상승(새벽 현상) 등 기존 검사로는 포착하기 어려운 정보를 제공합니다.
CGM을 통해 확인할 수 있는 주요 지표 중 ‘목표 혈당 범위 내 시간(Time in Range, TIR)’은 최근 혈당 변동성 관리의 새로운 기준으로 주목받고 있습니다. TIR은 하루 중 혈당이 70~180mg/dL 범위 안에 있는 시간의 비율로, 이 수치가 높을수록 혈당 변동성이 작다는 의미입니다. 최신 가이드라인에서는 TIR 70% 이상을 권장하고 있습니다.
CGM은 아직 비용 부담이 있고 모든 환자에게 필수적이지는 않습니다. 그러나 HbA1c가 목표 범위에 있음에도 인지 기능 변화가 의심되거나, 저혈당이 잦다거나, 혈당 조절이 잘 되지 않는다고 느끼는 분들에게 진료실에서 상담을 요청해볼 수 있는 도구입니다.
혈당 변동성 줄이는 실천법 — 기전과 기대 효과 요약
| 실천법 | 구체적 방법 | 작용 기전 | 기대 효과 |
|---|---|---|---|
| 식사 순서 변경 | 채소 → 단백질 → 탄수화물 순으로 섭취 | 식이섬유가 위에서 젤 형성 → 탄수화물 흡수 속도 지연 | 식후 혈당 스파이크 30~40% 감소 경향 |
| 식후 보행 | 식사 후 15~20분 이내 10~15분 걷기 | 근육 수축 → GLUT4 비인슐린 경로 활성화 → 혈당 흡수 | 식후 혈당 피크 높이와 지속 시간 감소 |
| 저혈당 예방 | 식사 거르지 않기, 운동 전후 혈당 확인 | 저혈당은 뇌 에너지 고갈 → 신경세포 직접 손상 | 인지 기능 저하 예방, 야간 저혈당 차단 |
| 수면 관리 | 하루 7~8시간 규칙적 수면 | 수면 부족 → 인슐린 저항성 증가 → 공복혈당 상승 | 혈당 변동성 감소, 아밀로이드 베타 뇌 청소 기전 유지 |
| CGM 모니터링 | 연속혈당측정기 착용, 변동 패턴 확인 | HbA1c가 정상이어도 스파이크 패턴 실시간 포착 | 식이·활동 습관 개선의 근거로 활용 |
| 오늘부터 시작할 수 있는 3가지 • 식사 순서를 바꿉니다 — 채소 먼저, 밥은 나중에. 식후 혈당 스파이크를 줄이는 가장 간단한 방법입니다 .• 밥 먹고 나서 바로 앉지 않습니다 — 식후 15분 이내에 10~15분 걷습니다. 근육이 혈당을 흡수합니다. • 저혈당 삽화가 잦다면 담당 의사에게 알립니다 — 과도한 혈당 강하가 뇌에 더 나쁠 수 있습니다. |
5. 당뇨 관리의 목표가 달라져야 합니다
당뇨 합병증 하면 흔히 망막병증, 신장병증, 말초신경병증을 떠올립니다. 이 합병증들은 오랜 시간에 걸쳐 천천히 진행되고, 조기 발견을 위한 정기 검사 체계도 잘 갖춰져 있습니다. 그러나 뇌 건강은 이 목록에서 상대적으로 소홀히 다루어져 왔습니다.
축적된 연구들이 말하는 것은 명확합니다. 당뇨 환자에서 인지 기능 저하는 생각보다 이른 시기부터 시작될 수 있으며, 혈당 평균값뿐 아니라 혈당이 얼마나 안정적으로 유지되느냐 — 변동성 — 가 뇌 건강을 결정하는 중요한 요인입니다. 식사 순서, 식후 보행, 수면 관리, 저혈당 예방은 신장과 눈을 위한 것이기도 하지만, 동시에 뇌를 위한 실천이기도 합니다.
진료실에서 당뇨 관리를 논의할 때 단순히 혈당 수치를 낮추는 것을 넘어, 혈당이 얼마나 안정적으로 유지되고 있는지를 함께 점검하는 것이 도움이 됩니다. 혼자 고민하기보다 진료를 통해 현재 패턴을 확인하고, 가장 적합한 관리 방향을 함께 정하는 과정이 필요합니다. 그 과정을 함께 가겠습니다.
고려할 사항
본 칼럼은 의학적 교육 목적으로 작성된 일반 정보입니다. 개별 환자의 진단, 혈당 목표치 설정, 약물 조정은 반드시 담당 의사의 직접 진료를 통해 결정되어야 합니다. 특히 저혈당 위험이 있는 분들은 혈당 관리 목표의 변경을 임의로 시도하지 않도록 권장합니다.
참고 문헌
1 Xue M, et al. Diabetes mellitus and risks of cognitive impairment and dementia: a systematic review and meta-analysis of 144 prospective studies. Ageing Res Rev. 2019;55:100944.
2 PMC 2024. Association between Age at Diagnosis of Type 2 Diabetes and Subsequent Risk of Dementia and Its Major Subtypes. NHIS Korea Cohort (N=612,201).
3 Rawlings AM, et al. HbA1c variability associated with dementia risk in people with type 2 diabetes. Alzheimers Dement. 2024; PMC11350038.
4 Lee et al. Fasting glucose variability and risk of dementia in 769,554 diabetic individuals. Korean Nationwide Cohort Study.
5 Testa A, et al. Cognitive dysfunction in diabetes: abnormal glucose metabolic regulation in the brain. Front Endocrinol. 2023;14:1192602.
6 Pugazhenthi S, et al. Alzheimer’s Disease as Type 3 Diabetes: Understanding the Link and Implications. Int J Mol Sci. 2024;25(22):11955.
7 Chin SO, et al. Hypoglycemia is associated with dementia in elderly patients with type 2 diabetes mellitus: Korea National Diabetes Program Cohort. Diabetes Res Clin Pract. 2016;122:54–61.
연관글
인기 건강 소식
비대면 진료
병원 방문이 어려운 경우에도 의료진과의
상담을 통해 필요한 진료를 이어갈 수 있습니다.
뉴스레터 구독
의료진이 직접 정리한 건강 관리 정보와
칼럼을 받아보실 수 있습니다.

